接上文,继续谈电池内部过程与控制方程的意义。
之前提到的过电位η与交换电流密度i0决定了电化学反应进行的程度,过电位η是反应的驱动力,在这里,我们定义:
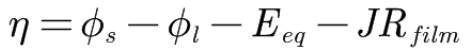
对于我们选定的电极,任意时刻的过电位与该电极的固相电势𝜙𝜙𝑠𝑠,液相电势𝜙𝜙𝑙𝑙,平衡电势Eeq,以及SEI膜电阻(负极)有关。初始时刻的过电位为0,我们可以在COMSOL Multiphysics中给定正负极的固、液相电势的初始值,使得两个多孔电极上的过电位为0。COMSOL锂离子电池接口求解的因变量有三个,其中就包括了固相电势𝜙𝜙𝑠𝑠和液相电势𝜙𝜙𝑙𝑙,所以我们可以得到给定区域过电位随时间的变化情况或者给定时刻的过电位随位置的变化情况,这些都是通过测试手段无法分析的,是软件模拟的优势之一。
交换电流密度i0反映的是一个电极反应得失电子的能力,以及可以反映一个电极反应进行的难易程度。其表达式较为复杂:
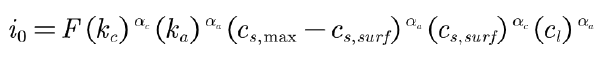
容易看出,交换电流密度与固相锂离子浓度与液相锂离子浓度有关,ka与kc是阴阳极电化学反应速率常数,单位是m/s,这是一个与温度关系密切的物理量,特别是在模拟电池低温性能的时候,如果反应速率常数不随温度变化,容易造成计算不收敛甚至无法计算,αa 与αc为阳极传递系数与阴极传递系数,单位是1,意义与Bulter—Volmer公式中意义相同。在反应速率常数不变的情况下,交换电流密度会随着固液相锂离子浓度的变化而变化,与电池的SOC(也就是固相锂离子表面浓度与最大固相浓度之比)相关。
3) 电解质中锂离子的传质过程(包括扩散与迁移)
如之前所述,在整个电解液内,包括隔膜和多孔电极,电解质中的锂离子传质过程采用Nernst—Planck方程描述,由于电池内部不考虑对流传质过程,简化后的方程如下:
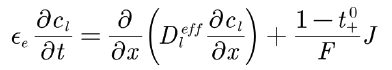
与之前的固相锂离子传质过程类似,方程的左边是液相浓度随时间的变化,εe表示电解液的体积分数,在后面的参数计算部分中我们会详细介绍电极体积分数与电解液体积分数的计算步骤。方程的右边有两项,第一项是扩散过程,与有效液相扩散系数与电解质盐浓度梯度有关;第二项是电迁移项,与离子流通量和电解液的迁移数有关。由于电解液中存在固液两相,因此我们需要在电解液与多孔电极的界面上添加连续性条件,保证电解液在电池内部连续。在这里,出现了锂电池接口内最后一个因变量,电解质盐浓度cl,不难发现,我们所需要的各种物理量例如发热功率,局部电流密度,电势分布曲线等都是通过这三个因变量计算得到的。
我们知道,电解液在多孔电极内的扩散不可能和隔膜区域内的相同,多孔电极内部的孔道结构越复杂,扩散越困难,因此我们需要对多孔电极内的电解质盐扩散系数进行修正,修正的方法是通过Bruggeman系数,修正的方法如下:
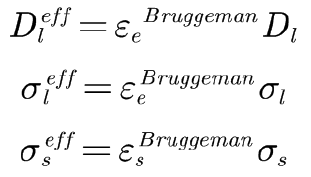
需要特别说明的是,一般而言液相的Bruggeman系数与固相的不相等,隔膜,正极和负极区域内的液相Bruggeman系数也不相等。正是由于Bruggeman系数的存在,使得多孔电极与电解液内部的扩散过程有了区别,在后面仿真结果分析中,我们可以明显看出电解质盐浓度在两个区域内变化的显著差异。
注:本文转载的是某乎ID“无话可说”大佬文章,由于文章内容已被移除,特在B站记录备份。更多comsol锂电仿真资料,请加Q群【940860203】